Ionentransport und elektrochemische Speicherung in kleinen Systemen ("Nano-Ionik")
Forschungsbericht (importiert) 2003 - Max-Planck-Institut für Festkörperforschung
Es ist modisch geworden, ein bestimmtes Fachgebiet durch das Präfix "nano" zu dekorieren, so sehr dass umgekehrt die ungestüme Verwendung desselben auch schon wieder diskreditierend wirken kann. Losgelöst von Voreingenommenheiten beiden Typs sollen im folgenden Beitrag einige unserer theoretischen und experimentellen Aktivitäten geschildert werden, deren Ansätze schon weit in die Anfänge unserer Arbeit auf dem Gebiet des Ionentransportes zurückgehen und deren Darstellung zwanglos deutlich werden lassen soll, dass in der Tat eine "Nano-Ionik" einer Nano-Elektronik im Hinblick auf fundamentale Bedeutung und Anwendungspotenzial an die Seite gestellt werden kann.
Während Elektronentransport in Chemie, Halbleiterphysik und Elektronik grundlegend ist für elementare Redoxvorgänge bis hin zur Wirkungsweise elektronischer Bauelemente, so gilt dies analogerweise für den Ionentransport (Ionik) in Hinblick auf Säure-Base-Vorgänge und elektrochemische Anwendungen wie Batterien, Brennstoffzellen oder chemische Sensoren, um nur die populärsten zu nennen. Während die Bedeutung von Randschichten in der Elektronik stets im Vordergrund stand, waren es fast ausschließlich die Stuttgarter Aktivitäten, die die Rolle der Grenzflächen für die Ionenleitung betonten. Im Nanometerregime, in dem die Abstände benachbarter Grenzflächen gerade mal so viele Atome betragen, dass zwar in der Regel typische Festkörpereigenschaften auftreten, sich aber benachbarte Grenzflächen in ihrer Wirkung häufig noch verspüren, treten typische mesoskopische Effekte auf, die auch qualitativ zu neuen Eigenschaften führen. Wir unterscheiden im Folgenden etwas salopp zwischen trivialen Größeneffekten, die ausschließlich auf der vergrößerten Anzahldichte der Grenzflächen beruhen, aber dennoch zuweilen sehr drastisch sind, wie z.B. das Umschlagen von Volumentransport in grenzflächenbestimmten Transport bei Verringerung der Korngröße einer Ionenleiterkeramik, und echten Größeneffekten, bei denen auch die lokale Situation durch Wechselwirkung zwischen der Grenzfläche verändert ist.
Ausgangspunkt ist das Verständnis des Ionentransports in Randschichten, vorrangig das Verständnis der Konzentration von ionischen Ladungsträgern in Randschichten. Wie bei Halbleitern erst Dotierung und thermische Energie frei bewegliche Elektronen sowie Elektronenlöcher als Ladungsträger entstehen lassen, sind auch beim perfekten Ionenkristall - wenn auch im Übermaß Ionen - so doch keine ionischen Ladungsträger vorhanden; Ionenleiter entstehen erst durch die Anwesenheit überschüssiger Ionen, die sich an anomalen Positionen des Kristallgitters befinden, bzw. von Leerstellen, d.h. unbesetzten regulären Gitterpositionen; auch diese werden durch Dotierung oder thermische Energie erzeugt. Wie wir in vielen Beispielen experimentell und theoretisch gezeigt haben, treten an Randschichten enorme Variationen dieser ionischen Ladungsträgerkonzentrationen auf, wie dieses auch in der Halbleiterphysik in Bezug auf die elektronischen Ladungsträger bekannt ist. Von uns untersuchte Beispiele sind die Umverteilung von Ionen an Kontakten zweier Ionenleiter, an Korngrenzen polykristalliner Stoffe, an der Phasengrenze zu aktiven Gasphasen oder am Kontakt mit festen oberflächenaktiven Isolatoren. Die Ausdehnung der Zone, innerhalb dieser sich solche Prozesse abspielen, ist durch die so genannte Debye-Länge gegeben; ist der Abstand der Grenzflächen kleiner als diese Größe, überlappen sich die Raumladungszonen, und ein echter Größeneffekt tritt auf.
Im Folgenden sollen eine Reihe von aktuellen Beispielen aus unserem Arbeitskreis die enorme Relevanz dieser Phänomene darlegen.
Eine neue Klasse weicher Elektrolyte: "Soggy Sand Electrolytes"
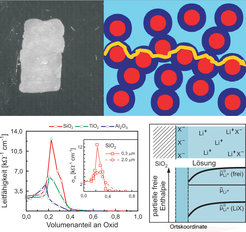
Für die Anwendung (Lithium-Batterien) äußerst wichtige Elektrolyte sind nichtwässrige flüssige Ionenleiter, typischerweise bestehend aus in organischen Lösemitteln aufgelösten Lithiumsalzen. In aller Regel besitzen solche nichtwässrigen Lösemittel eine geringe Dielektrizitätskonstante, was eine nichtvollständige Dissoziation der Lithiumsalze zur Folge hat. Vordergründig paradoxerweise, aber im Sinne unserer Arbeiten an festen Ionenleitern folgerichtig, führt das Einbringen von isolierenden SiO2-Partikeln nicht nur zu den günstigen mechanischen Eigenschaften "weicher Materie", sondern auch zu deutlich erhöhter ionischer Leitfähigkeit. Die sauren SiO2-Partikel adsorbieren nämlich die Anionen und setzen damit mobile Lithium-Ionen aus den gebundenen Assoziatzuständen frei (Abb. 1). Dies führt zu signifikanten Leitfähigkeitserhöhungen, z.B. im System LiClO4/MeOH. Ähnliche Effekte treten auch in typischen Batterieelektrolyten wie LiPF6 in Ethylencarbonat/Dimethylcarbonat auf, was die Anwendungsrelevanz dieser neuen Elektrolyte verdeutlicht. Bei Volumenanteilen von über 10% können die Partikelabstände unabhängig von der Salzkonzentration durchaus die Debye-Länge unterschreiten, sodass es sich weitgehend um mesoskopische Ionenleiter handelt.
Künstliche mesoskopische Ionenleiterübergitter
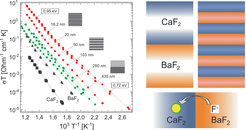
Sehr elegant lassen sich Raumladungseffekte an den von uns durch Molekularstrahlepitaxie hergestellten Ionenleiterübergitter demonstrieren und untersuchen, welche abwechselnd aus Schichten von BaF2 und CaF2 aufgebaut sind (Abb. 2). Wie eingangs erwähnt, verlangt das Kontaktgleichgewicht eine Umverteilung von mobilen F--Ionen auf Kosten einer elektrischen Aufladung. Dieser Umverteilung zufolge wird auf einer Seite die Konzentration an zusätzlichen F--Ionen (Zwischengitterionen) und auf der anderen Seite die Konzentration an Leerstellen erhöht, beides führt zu einer erhöhten Leitfähigkeit entlang der Grenzfläche. Da die Dicke der einzelnen Schichten zwischen 1 nm und 1 mm variiert werden kann, können die Größeneffekte präzise studiert werden. Abbildung 2 zeigt das Anwachsen der Leitfähigkeit allein durch das Einbringen von Grenzflächen; die Leitfähigkeit wächst auch in einem Bereich, in dem die Debye-Länge oberhalb des Grenzflächen-Grenzflächen-Abstands liegt; im Sinne eines echten Größeneffektes überlappen hier die Raumladungszonen. Als Extremfall solcher Schichten mögen auch Stapelfehlerarrangements im AgI dienen, die als Schichtpakete von γ-AgI auf β-AgI aufgefasst werden können und an welchen wir anomal hohe Ag+-Ionenleitfähigkeit entdeckten.
Ionenblockade in Verarmungsrandschichten
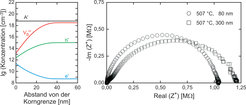
Neben der Akkumulation von ionischen Ladungsträgern haben wir auch eine gezielte Verarmung von ionischen Ladungsträgern erreichen können. Dies ist z.B. an Korngrenzen von SrTiO3 möglich (Abb. 3). Eine qualitative Konsequenz ist beispielsweise die Blockade des Sauerstofftransports bei elektrischen oder chemischen Experimenten. Wählt man so genannte Kleinwinkelkorngrenzen, tritt ein innerer Größeneffekt auf: Solche Kleinwinkelkorngrenzen können als Netzwerk von Versetzungskernen beschrieben werden, wobei in unserem Falle diese Kerne positiv und die Umgebung negativ geladen ist. Aufgrund der engen Nachbarschaft überlagern sich die Einflusszonen, und ein homogener Blockadeeffekt tritt in Erscheinung.
Ist die Dichte der Korngrenzen hoch genug, können diese Raumladungszonen auch die gesamten Körner durchdringen und im Innern zur Verarmung führen. Diesen nicht-trivialen Größeneffekt (Abb. 3), der das Gegenstück zur Anreicherungssituation in den Übergittern (Abb. 2) darstellt, haben wir in dichtgesinterten, nanokristallinen SrTiO3-Keramiken beobachtet. Die elektrostatischen Effekte werden in diesem Fall von elastischen Phänomenen begleitet, die sich in einem weiteren, nun aber dielektrischem Größeneffekt manifestieren. Im Gegensatz zum SrTiO3-Einkristall oder zu mikrokristallinem SrTiO3 werden diese dichten nanokristallinen Keramiken, vermutlich aufgrund von Verspannungseffekten, offenbar ferroelektrisch.
Inversionsrandschichten in nanokristallinem CeO2
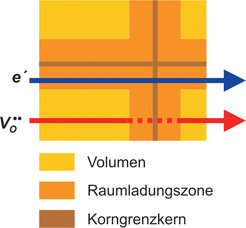
Das gleiche Phänomen, das beim SrTiO3 in einer Verringerung der Konzentration der (positiv geladenen) Sauerstoffleerstellen und der (positiv geladenen) Elektronenlöcher resultiert, führt zur Erhöhung der Konzentration der (negativ geladenen) Überschusselektronen (Leitungselektronen). In nanokristallinem CeO2 ist die Elektronenkonzentration hoch genug und gleichzeitig die Grenzflächendichte so groß, dass die gesamte Keramik n-leitend wird, obwohl im Korninnern Ionenleitung überwiegt (Abb. 4).
Nanogrößeneffekt in Lithium-Batterie-Elektroden: Ein neuer Speichermechanismus
Lithium-Batterien sind als typische Raumtemperaturanwendungen sehr geeignet, um das technologische Potenzial einer Nano-Ionik zu demonstrieren. Als eindrucksvolles Beispiel wurden schon die "Soggy Sand Electrolytes" erwähnt. Ein anderer Aspekt bezieht sich auf die Elektroden. Typische Elektroden in Lithium-Batterien sind so genannte Interkalationselektroden (typischerweise Übergangsmetalloxide), in die das durch die elektrochemische Zelle überführte Lithium ohne Änderung der Struktur untergebracht werden kann. Naturgemäß ist die Unterbringungskapazität dann sehr begrenzt. Im Prinzip kann deutlich mehr Lithium unter Energiegewinn überführt werden, allerdings auf Kosten der Ausbildung eines Gemenges mehrerer Phasen (nämlich bis zur Reduktion zum Metall oder gar einer Li-Legierung unter Bildung von Li2O). Bei solchen heterogenen Festkörpersystemen würde aber beim Laden der Batterie der ursprüngliche Zustand nur unvollkommen und sehr zögerlich wiederhergestellt. Wie verschiedene Arbeitsgruppen weltweit gezeigt haben, ist dies aber möglich, wenn die Partikel im Phasengemenge sehr klein sind, also ein Nanokomposit vorliegt (Abb. 5).
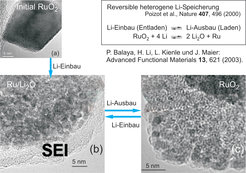
Überdies lässt sich offenbar anomal viel Lithium in Grenzflächen reversibel speichern. Unserem Verständnis zufolge liegt auch diesem Phänomen ein elektrischer Doppelschichteffekt zugrunde (Abb. 3). Ist RuO2 die Ausgangselektrode, liegt nach Einbringen von mehr als 1 Li pro RuO2 ein Phasengemisch aus Li2O und Ru vor. Li2O kann nicht in nennenswerter Weise Li aufnehmen, nicht weil Lithium-Ionen nicht aufgenommen werden könnten (es gibt eine Vielzahl unbesetzter Zwischengitterplätze), es ist hierfür allein die Tatsache wesentlich, dass keine Elektronen aufgenommen werden können (Li=Li++e-). Tritt aber eine an den Ru/Li2O-Grenzflächen mögliche "Arbeitsteilung" ein (Li+-Aufnahme oxidseitig, e--Aufnahme metallseitig), wird eine Lithium-Speicherung ermöglicht, und dies im nanokristallinen Zustand in durchaus merklichem Ausmaße. Insbesondere ist der Kapazitätsgewinn deutlich, wenn die Debye-Länge größer als die Partikelgröße ist. Dann verwischt dieser Größeneffekt den Unterschied zwischen elektrostatischem Kondensator und Batterieelektrode.
Strukturelle Größeneffekte, Kapillareffekte und andere
Naturgemäß lassen sich nicht alle Effekte und Ionenleitungsanomalien auf reine Raumladungsphänomene zurückführen. In einigen der schon gezeigten Beispiele sind auch teilweise Veränderungen der lokalen energetischen Lage (Energieniveaus) maßgeblich, insbesondere bei elastischen Verspannungen größerer Reichweite. Grundsätzlich wichtig werden Effekte auf die Energieniveaus, wenn die Einflusssphäre eines Ladungsträgers von der Größenordnung der Abstände der Grenzflächen ist. Bei delokalisierten Elektronen ist das bekanntlich schon bei großen Abständen der Fall. So ist ein zukünftig wichtiges Aufgabenfeld unserer Abteilung die Erforschung von Größeneffekten so genannter gemischter Leiter, die sowohl ionische als auch elektronische Leitfähigkeit in merklichem Ausmaß aufweisen. Ein Punkt, der bei dünnen Filmen nicht, wohl aber bei gekrümmten Grenzflächen, von Bedeutung ist, ist der erhöhte Binnendruck im Teilcheninnern, wie er ja auch bei Seifenblasen bekannt ist. Auch dieser beeinflusst die Ladungsträgerverteilung, ja induziert erst eine solche, wenn es sich um den Kontakt chemisch identischer, aber verschieden großer Partikel handelt. Dass solche Kapillaritätsphänomene von außerordentlicher Wichtigkeit sind, zeigt das bekannte Absenken des Schmelzpunktes von Metallen mit der Korngröße, aber auch das Verschieben der Stabilitätsabfolge verschiedener TiO2-Modifikationen mit der Korngröße. Unseren Messungen zufolge wird - bei herkömmlichen Herstellungstemperaturen - der üblicherweise metastabile Anatas zur thermodynamisch stabileren Modifikation, wenn die Korngröße 10 nm unterschreitet. Die Stabilitätsdifferenz beider Oxide kann unmittelbar an der Spannung einer von uns entwickelten elektrochemischen Zelle abgelesen werden.
Wir sind der Überzeugung, und wir hoffen auch den Leser mithilfe dieser wenigen aktuellen Fallstudien überzeugt zu haben, dass eine Nano-Ionik mehr darstellt als ein modisch benanntes Fachgebiet, sondern ähnlich wie die Nanoelektronik der modernen Materialforschung neue Perspektiven eröffnet.
Literatur
[1] Bhattacharyya, A. J. und J. Maier: Advanced Materials 16, 811 (2004).
[2] Sata, N., K. Eberman, K. Eberl und J. Maier: Nature 408, 946 (2000).
[3] De Souza, R. A., J. Fleig, R. Merkle und J. Maier: Zeitschrift für Metallkunde 94, 218 (2003); Balaya, P. et al., in Vorbereitung.
[4] Kim, S. und J. Maier: Journal of The Electrochemical Society 149, J73 (2002).
[5] Balaya, P., H. Li, L. Kienle und J. Maier: Advanced Functional Materials 13, 621 (2003); Jamnik, J. und J. Maier: Physical Chemistry Chemical Physics 5, 5215 (2003).
!["Soggy Sand Electrolytes": Zum Mechanismus und Ausmaß der Leitfähigkeitserhöhung [1]. Die rechte Seite (unten) zeigt die Übersetzung der Situation in ein Energiediagramm. "Soggy Sand Electrolytes": Zum Mechanismus und Ausmaß der Leitfähigkeitserhöhung [1]. Die rechte Seite (unten) zeigt die Übersetzung der Situation in](https://www.mpg.de/828047/original-1294357442.jpg?t=eyJ3aWR0aCI6MzQxLCJmaWxlX2V4dGVuc2lvbiI6ImpwZyIsIm9ial9pZCI6ODI4MDQ3fQ%3D%3D--db934b401e47b5ace224a076acf7b2a1775b1c3c)
![Mesoskopische Ionenleiterübergitter: Mechanismus (rechts) und temperaturabhängige Leitfähigkeit (links) als Funktion der Grenzflächenabstände [2]. Mesoskopische Ionenleiterübergitter: Mechanismus (rechts) und temperaturabhängige Leitfähigkeit (links) als Funktion der Grenzflächenabstände [2].](https://www.mpg.de/828103/original-1294357381.jpg?t=eyJ3aWR0aCI6MzQxLCJmaWxlX2V4dGVuc2lvbiI6ImpwZyIsIm9ial9pZCI6ODI4MTAzfQ%3D%3D--38acf458426a056057e1b7b28a392735930bb7b1)
![Verarmungsrandschichten für elektronische (Löcher, h•) und ionische (Leerstellen, V••) Ladungsträger für eine isolierte SrTiO3-Korngrenze sowie in nanokristallinem SrTiO3. Im Impedanzspektrum (rechts) zeigt sich das Verschwinden des Volumenanteils [3]. Verarmungsrandschichten für elektronische (Löcher, h•) und ionische (Leerstellen, V••) Ladungsträger für eine isolierte SrTiO3-Korngrenze sowie in nan](https://www.mpg.de/828159/original-1294357360.jpg?t=eyJ3aWR0aCI6MzQxLCJmaWxlX2V4dGVuc2lvbiI6ImpwZyIsIm9ial9pZCI6ODI4MTU5fQ%3D%3D--a80e9d6afa006ed875b44ade435ce0c527695799)
![Mechanismus der Elektronen- (Leitungselektronen, e′) und Ionenleitfähigkeit (Leerstellen, V••) in nanokristallinem CeO2 [4]. Mechanismus der Elektronen- (Leitungselektronen, e′) und Ionenleitfähigkeit (Leerstellen, V••) in nanokristallinem CeO2 [4].](https://www.mpg.de/828215/original-1294357494.jpg?t=eyJ3aWR0aCI6MzQxLCJmaWxlX2V4dGVuc2lvbiI6ImpwZyIsIm9ial9pZCI6ODI4MjE1fQ%3D%3D--2ae5717034a2631a1d6456e4fb99a525809e68f9)
![Hochaufgelöste Transmissionselektronenbilder (Kienle, Abteilung Simon) von RuO2-Elektroden. Bei Li-Aufnahme zerfällt der Kristall in einen Li2O/Ru-Komposit, aus dem reversibel Li extrahiert werden kann. Aufgrund elektrischer Doppelschichteffekte kann zusätzlich Li in den Grenzflächen des Komposits gespeichert werden [5]. Hochaufgelöste Transmissionselektronenbilder (Kienle, Abteilung Simon) von RuO2-Elektroden. Bei Li-Aufnahme zerfällt der Kristall in einen Li2O/Ru-Kom](https://www.mpg.de/828271/original-1294357479.jpg?t=eyJ3aWR0aCI6MzQxLCJmaWxlX2V4dGVuc2lvbiI6ImpwZyIsIm9ial9pZCI6ODI4MjcxfQ%3D%3D--6a989b684664ca6f597a54b2475e1c395a0d54a8)